Un projet pilote pour les cancers
MULTIPLI est le programme de projets pilotes des cancers du plan France médecine génomique 2025.
Le programme s'inscrit également dans le cadre du plan cancer.
Pourquoi séquencer une tumeur ?
Anomalies génétiques et cancer
Le cancer résulte de l’accumulation dans l’ADN d’anomalies de plusieurs types : mutations ponctuelles d’une base nucléique, insertion/délétion (InDel) d’un petit nombre de bases, et plus rarement amplification/délétion ou translocation d’une séquence génomique. Ces anomalies entraînent une modification de l’expression des gènes qui les portent, ce qui entraîne le déclenchement et la progression du processus cancéreux.
Ces anomalies génétiques ne concernent pas seulement les cancers héréditaires, dans lesquels l’anomalie génétique, souvent connue, est présente dans l’ADN de toutes les cellules (ADN constitutionnel). L’ADN des cellules cancéreuses présente en effet diverses anomalies acquises, dites somatiques, qui sont absentes de l’ADN des cellules saines. Le nombre d’anomalies somatiques identifiées augmente au fur et à mesure des progrès de la recherche. Elles sont recensées dans des bases de données régulièrement mises à jour et consultables par l’ensemble de la communauté médicale et scientifique internationale.
Les gènes portant des anomalies génétiques sont dits driver de la maladie lorsque leur expression ou leur absence d’expression anormales dans la cellule est associée à l’initiation et au maintien du cancer. Les anomalies sont elles-même dites driver quand elles ont un effet direct, activateur ou inhibiteur, sur l’expression de ces gènes. Certaines anomalies génétiques driver entraînent quant à elles la fusion de séquences génomiques, avec pour conséquence la production de transcrits de fusion identifiables par une étude de l’ARN.
Le séquençage à très haut débit (NGS, Next generation sequencing) permet aujourd’hui de séquencer des génomes plus rapidement qu’auparavant et à un coût moindre. Il est donc possible de mener des études sur un nombre de plus en plus important d’échantillons tumoraux, ce qui a un intérêt :
- en termes de recherche, afin d’améliorer la connaissance des gènes et de leurs produits (les protéines) impliqués dans les processus de cancérogenèse ;
- en termes de soin, afin d’adapter la prise en charge des patients aux caractéristiques génétiques de leur tumeur : c’est le concept de médecine génomique, qui appartient au domaine de la médecine de précision.
Anomalies génétiques et thérapies ciblées
L’identification d’anomalies génétiques driver au sein des tumeurs s’accompagne du développement de thérapies anticancéreuses ciblées. Ces traitements utilisent des molécules susceptibles de contrecarrer les effets d’une anomalie génétique, alors dite actionnable, ralentissant ainsi, voire stoppant, le processus cancéreux. Les traitements ciblés ne sont pas nécessairement plus efficaces que les traitements conventionnels, mais ils permettent d’élargir l’arsenal thérapeutique. Ils présentent notamment un intérêt pour les patients atteints de cancers avancés ou résistants aux thérapies conventionnelles de première ligne, ou en combinaison thérapeutique.
Aujourd’hui, de tels traitements ciblés existent pour une quinzaine d’anomalies génétiques somatiques. La recherche de ces anomalies, désormais réalisée par séquençage à très haut débit (NGS) afin d’augmenter le nombre de patients pouvant en bénéficier, est assurée sur l’ensemble du territoire grâce aux 28 plateformes de génétique moléculaire labellisées par l’Institut national du cancer (INCa). Le séquençage porte sur un ensemble de gènes (un panel de gènes) susceptibles de présenter ces anomalies. La détection d’une de ces anomalies permet alors de proposer au patient le traitement ciblé correspondant.
Objectifs de MULTIPLI
Les cancers sont loin d’être tous caractérisés par les anomalies génétiques connues actuellement recherchées. De plus, les caractéristiques génétiques d’une tumeur sont probablement très spécifiques à un individu donné. Pour augmenter les chances de détecter chez un patient des anomalies génétiques encore inconnues et potentiellement actionnables, il est nécessaire d’étendre le séquençage à un plus grand nombre de gènes, voire à l'exome tumoral et même à l'intégralité du génome tumoral. Parallèlement, l'étude de l’ensemble du transcriptome tumoral doit permettre d’analyser dans sa globalité l’expression du génome dans la cellule cancéreuse.
Aujourd’hui, le séquençage à très haut débit de l’exome (WES, Whole exome sequencing) et du transcriptome (RNASeq) tumoraux est encore du domaine de la recherche. Des études sont nécessaires pour tester in situ sa capacité à être intégré dans la routine clinique : c'est l'objectif principal du programme MULTIPLI.
Faisabilité du NGS en routine
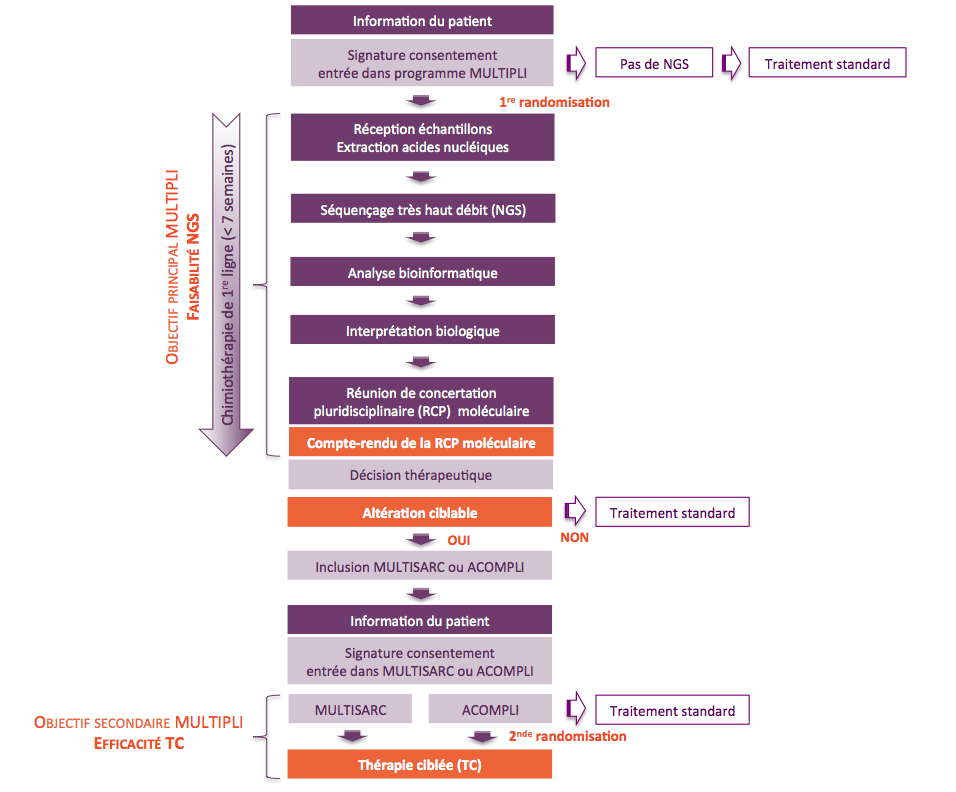
Le programme MULTIPLI a pour mission d’identifier et lever les verrous technologiques, cliniques et réglementaires bloquant la mise en œuvre du séquençage tumoral à très haut débit (NGS) chez un grand nombre de patients (échelle du territoire national) et dans un délai restreint, celui de la durée du traitement de première ligne des patients (7 semaines maximum).
La faisabilité du NGS sera évaluée en mesurant "la proportion de patients pour lesquels les résultats du séquençage sont interprétables et sont transmis sous forme d’un compte-rendu et d’une recommandation thérapeutique de la réunion de concertation pluridisciplinaire (RCP) moléculaire à l’investigateur dans un délai de 7 semaines suivant la réception des échantillons (sanguins et tumoraux) par l’une des plateformes de génétique moléculaire de MULTIPLI labellisée par l'INCa".
Dans un premier temps, l’analyse des données de séquence réalisée dans le délai de 7 semaines concernera :
Pour les anomalies somatiques :
- 90 gènes cibles des molécules disponibles dans le programme MULTIPLI ;
- 616 gènes connus pour être impliqués dans la cancérogenèse (Cancer Gene Census) ;
- les transcrits de fusion (analyse du transcriptome tumoral) ;
Pour les anomalies constitutionnelles :
- 59 gènes porteurs d’éventuelles anomalies incidentes germinales (ACMG) ;
- les polymorphismes génétiques associés à un risque plus élevé de toxicité médicamenteuse (PharmGKB).
L’analyse de l’exome entier sera réalisée dans un second temps, hors des objectifs de Multipli.
Efficacité des traitements ciblés innovants proposés dans MULTIPLI
La présence d’une anomalie génétique actionnable ne permet pas, à elle seule, de prédire avec certitude une réponse à un traitement ciblé. De plus, si cette réponse existe, elle n'est pas obligatoirement supérieure à celle obtenue avec le traitement conventionnel le plus efficace. C'est la réalisation d'un essai clinique qui permet d’évaluer l’efficacité d’un traitement ciblé innovant pour un cancer donné.
Les essais cliniques composant MULTIPLI concernent deux types de cancer qui diffèrent par leur fréquence, leur pronostic et l’arsenal thérapeutique disponible pour chacun d’eux :
- le sarcome des tissus mous avancé (essai MULTISARC);
- le cancer colorectal métastatique (essai ACOMPLI).
L'objectif secondaire du programme MULTIPLI (et donc des essais MULTISARC et ACOMPLI) est d'évaluer l'efficacité des traitements ciblés innovants proposés dans le partenariat public/privé de MULTIPLI. Il s'agit :
- soit de nouvelles molécules,
- soit de molécules existantes, mais qui n’ont pas encore été testées dans les indications des essais MULTISARC et ACOMPLI (sarcomes des tissus mous avancés ou cancers colorectaux métastatiques).
Ces molécules seront évaluées chez les patients dont le séquençage à très haut débit du génome tumoral a mis en évidence les anomalies génétiques cibles de ces molécules. Leur efficacité clinique sera comparée à celle du traitement standard le plus efficace.